 林榮俊助理教授於2008年1月取得臺灣大學分子醫學研究所博士學位,隨後在中央研究院生物醫學科學研究所譚婉玉研究員實驗室擔任博士後研究學者,於2012年2月至臺北醫學大學醫學檢驗暨生物技術學系任教。(編按)
林榮俊助理教授於2008年1月取得臺灣大學分子醫學研究所博士學位,隨後在中央研究院生物醫學科學研究所譚婉玉研究員實驗室擔任博士後研究學者,於2012年2月至臺北醫學大學醫學檢驗暨生物技術學系任教。(編按)
 截至目前研究發現,在人類細胞中超過90%的訊息RNA(messenger RNA)會藉由替代性剪接(alternative splicing)的機制,造成基因表現的多樣性,這種現象在不同的組織中或發育時期,受到嚴密的調控以符合生理功能。當訊息RNA的替代性剪接機制發生錯誤時,其產生錯誤的蛋白質亞型不但會造成多種遺傳疾病,也是造成正常細胞癌化的重要起因之一。
截至目前研究發現,在人類細胞中超過90%的訊息RNA(messenger RNA)會藉由替代性剪接(alternative splicing)的機制,造成基因表現的多樣性,這種現象在不同的組織中或發育時期,受到嚴密的調控以符合生理功能。當訊息RNA的替代性剪接機制發生錯誤時,其產生錯誤的蛋白質亞型不但會造成多種遺傳疾病,也是造成正常細胞癌化的重要起因之一。
細胞中的mRNA都會形成巨大的核糖核酸蛋白複合物。此類複合體可以負責不同的功能,例如mRNA的轉譯後修飾、胞內運輸或定位。第4號有氧核醣核酸結合蛋白(RNA binding protein motif protein 4;RBM4)具有兩個RNA結合區域,在先前的實驗結果證明RBM4在細胞核中扮演可調控訊息RNA發生替代性剪接的剪接因子(splicing factor)。【圖:林榮俊助理教授】
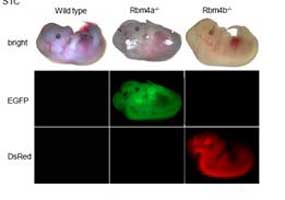 RBM4在大多數的組織中都會表現,但是在橫紋肌,中樞神經與睪丸中的表現量遠高於其他組織。先前的研究證實,RBM4在乙型胰島的前驅細胞中會藉由調控胰島素受體的替代性剪接,進而促進乙型胰島的發育,而RBM4的基因剔除小鼠為第一型糖尿病的動物模式。於今年發表的論文中,證明大量表現的RBM4蛋白可調控脂肪母細胞中一系列基因的替代性剪接,使其分化為具有高代謝活性的棕色脂肪細胞。【圖:RBM4剔除的小鼠胚胎】
RBM4在大多數的組織中都會表現,但是在橫紋肌,中樞神經與睪丸中的表現量遠高於其他組織。先前的研究證實,RBM4在乙型胰島的前驅細胞中會藉由調控胰島素受體的替代性剪接,進而促進乙型胰島的發育,而RBM4的基因剔除小鼠為第一型糖尿病的動物模式。於今年發表的論文中,證明大量表現的RBM4蛋白可調控脂肪母細胞中一系列基因的替代性剪接,使其分化為具有高代謝活性的棕色脂肪細胞。【圖:RBM4剔除的小鼠胚胎】
 目前實驗室主要的研究方向分為:
目前實驗室主要的研究方向分為:
1.藉由次世代定序針對轉譯組進行分析找出更多受RBM4調控而發生替代性剪接的基因,進而對棕色脂肪細胞的分化機制能有更深刻的了解。
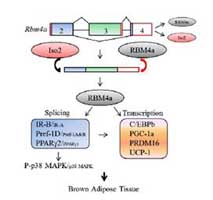
2.同樣藉由次世代定序針對轉譯組進行分析,探討RBM4在癌症細胞中是否調控特定基因的替代性剪接,以及此事件對細胞癌化的影響為何。(文/林榮俊,醫學科技學院醫學檢驗暨生物技術學系助理教授)【圖:RBM4蛋白藉由調控特定基因之替代性剪接,促進棕色脂肪細胞分化之機制】
●《Biochimica et Biophysica Acta》〈Emerging role for RNA binding motif proftein 4 in the development of brown adipocytes〉

