 謝嘉玲老師畢業於臺灣大學醫事檢驗學系學士班及碩士班,同校微生物暨免疫學博士班。曾任美國維吉尼亞大學(University of Virginia)泌尿科博士後研究員,埃默瑞大學(Emory University)醫學院泌尿科助理教授,其研究專長在於研究癌症轉移的機制與發展癌症之基因治療策略。
謝嘉玲老師畢業於臺灣大學醫事檢驗學系學士班及碩士班,同校微生物暨免疫學博士班。曾任美國維吉尼亞大學(University of Virginia)泌尿科博士後研究員,埃默瑞大學(Emory University)醫學院泌尿科助理教授,其研究專長在於研究癌症轉移的機制與發展癌症之基因治療策略。
 2007年因應中國醫藥大學癌症生物學研究所成立回國擔任該所副教授一職。2013年應聘至本校轉譯醫學博士學位學程任教,期待在這塊優質的教育園地中持續擔任一位稱職的園丁,滋育學生,幫助他們創造屬於自己不一樣的未來。(編按)
2007年因應中國醫藥大學癌症生物學研究所成立回國擔任該所副教授一職。2013年應聘至本校轉譯醫學博士學位學程任教,期待在這塊優質的教育園地中持續擔任一位稱職的園丁,滋育學生,幫助他們創造屬於自己不一樣的未來。(編按)
間葉幹細胞是近年來熱門的研究課題之一,主要原因在於它的體外增殖及多重分化能力,因此認為極具治療各種疾病的潛力。我們近期研究重點則在於探討間葉幹細胞生物特性和分化機制與癌症方面的相關性、以及幹細胞臨床應用技術研究。【圖:謝嘉玲老師】
實驗室先前已研發一新型的溶瘤腺病毒Ad-hOC-E1,利用骨鈣素啟動子選擇性的讓病毒只在癌細胞中複製,並可藉由vitamin D3的誘導增強癌細胞毒殺效力。雖然在小鼠的實驗動物模型中驗證其治療腫瘤的效果,但是組織啟動子容易造成正常細胞的非特異毒性,而高腫瘤特異性的啟動子其轉錄效率通常相對薄弱,因此溶瘤病毒在目前臨床試驗的療效仍有限。
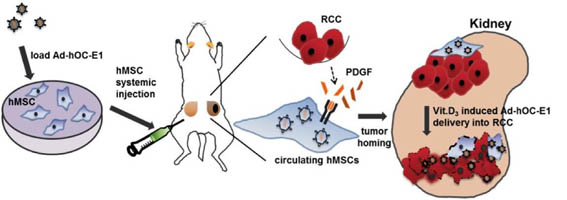
為此實驗室最近利用骨髓間葉幹細胞具有移行到腫瘤位置的特性將其作為攜帶溶瘤腺病毒的細胞載體。在腎癌的動物模型中,證實以全身性注射攜帶Ad-hOC-E1的間葉幹細胞在配合vitamin D3的給予,能明顯的抑制腫瘤在裸鼠體內生長達到治療效果;同時也發現間葉幹細胞對腎癌趨向性機制是藉由癌細胞釋放出的PDGF-AA來激活PDGF受體。此項研究成果可望促成溶瘤腺病毒在癌症標靶治療的臨床應用。【下圖:誘導型間葉幹細胞載體在溶瘤腺病毒癌症治療的應用】
 另一方面,由於骨轉移和骨骼併發症是前列腺癌的發病率和死亡率的主要因素。研究團隊為了解前列腺癌細胞如何調控這個病程,最近利用一個體外三維細胞共培養模型,建立起成對的正常和腫瘤周邊的骨髓間葉幹細胞株。
另一方面,由於骨轉移和骨骼併發症是前列腺癌的發病率和死亡率的主要因素。研究團隊為了解前列腺癌細胞如何調控這個病程,最近利用一個體外三維細胞共培養模型,建立起成對的正常和腫瘤周邊的骨髓間葉幹細胞株。
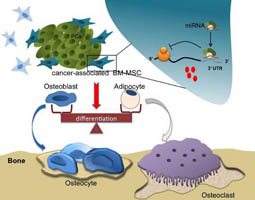
在體外和實驗動物模型中證實,除了癌細胞本身的病變外,腫瘤周邊的骨髓間葉幹細胞也會經由與癌細胞間的相互作用,改變自己微型核糖核酸(microRNA)的生成來調控基因的表現,以促進腫瘤的生長及轉移。
而癌細胞也可藉由改變骨髓間葉幹細胞成骨/成脂譜系的分化,趨向促成骨髓非正常型的成骨或蝕骨性病變。未來希望藉由找出骨髓間葉幹細胞調控病理骨重塑的致病因子,來研發一個新型治療策略,能有效阻斷並清除前列腺癌骨轉移。(文/謝嘉玲,醫學科技學院轉譯醫學博士學位學程副教授)【圖:骨髓間葉幹細胞調控前列腺癌骨重塑的機制】

