李松柏助理教授在國防大學生命科學研究所攻讀博士學位時,於中央研究院基因體研究中心阮麗蓉教授實驗室進行論文研究,2009年取得博士學位後,於2011年前往丹麥哥本哈根大學的生物科技研究與創新中心(Biotech Research and Innovation Centre, BRIC)進行博士後研究,並於2016年進入臺北醫學大學藥學院臨床藥物基因體學暨蛋白質體學碩士學位學程擔任助理教授。(編按)
李松柏助理教授在國防大學生命科學研究所攻讀博士學位時,於中央研究院基因體研究中心阮麗蓉教授實驗室進行論文研究,2009年取得博士學位後,於2011年前往丹麥哥本哈根大學的生物科技研究與創新中心(Biotech Research and Innovation Centre, BRIC)進行博士後研究,並於2016年進入臺北醫學大學藥學院臨床藥物基因體學暨蛋白質體學碩士學位學程擔任助理教授。(編按)
 維持生物體的正常發育及功能,仰賴著細胞對其生長、分化及死亡的精準調控。當DNA進行複製時,染色質中的去氧核糖核酸序列及其表觀遺傳訊息必須完整且準確地傳遞至子代細胞。若這些訊息在複製過程中無法被保留,將導致基因突變且破壞基因體的穩定性,進而引發嚴重的疾病,例如癌症。
維持生物體的正常發育及功能,仰賴著細胞對其生長、分化及死亡的精準調控。當DNA進行複製時,染色質中的去氧核糖核酸序列及其表觀遺傳訊息必須完整且準確地傳遞至子代細胞。若這些訊息在複製過程中無法被保留,將導致基因突變且破壞基因體的穩定性,進而引發嚴重的疾病,例如癌症。
為了探索人類細胞內調控DNA複製的機轉,本研究團隊發展出「新合成染色質純化技術」(Nascent Chromatin Capture, NCC);先使用去氧核糖核酸的類似物標記複製中的染色質,再利用生化方法分離出被標記的染色質及附著於其上的蛋白質複合體。藉由質譜儀分析,已純化出 3,995個蛋白質,其中包含完整的DNA複製體(Replisome)及近500個控制染色質結構的因子,且發現93個未曾被報導與DNA複製有關的新因子。此研究成果已發表於《自然細胞生物學期刊》(Nature Cell Biology),是染色質複製的研究領域的一大突破 。【右圖:李松柏助理教授】
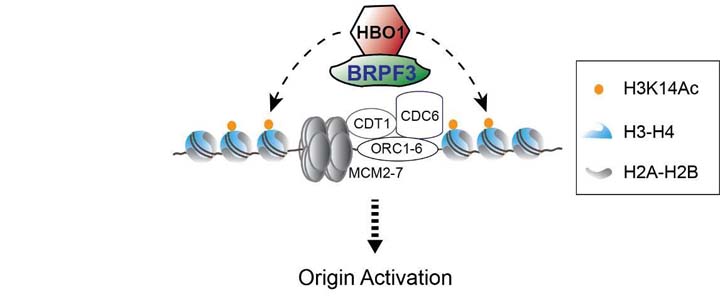
另一方面,研究團隊也利用小干擾核糖核酸篩選技術(siRNA screen)找到了20個具調控DNA複製能力的新因子,經生物統計學的分析及整合相關文獻後,再聚焦於探討BRPF3(bromodomain‐and PHD finger‐containing protein 3)在DNA複製時所扮演的角色。研究結果發現BRPF3會結合於DNA複製的起始點,並促進DNA複製初期的起始點活化反應,這可能是BRPF3吸引乙醯轉移酶HBO1至該位置對染色質中的組蛋白進行乙醯化反應所造成(圖2)。此研究成果已發表在歐洲《分子生物組織期刊》(The EMBO Journal)。
實驗室未來的研究將繼續找尋調控DNA複製的新機制及訊息傳遞網絡,並藉由小分子的篩選實驗,找出可破壞腫瘤細胞的基因體穩定性的藥物,期望能為癌症病患提供新的治療方向。(文/李松柏,藥學院臨床藥物基因體學暨蛋白質體學碩士學位學程助理教授)【下圖:BRPF3會結合於DNA複製的起始點,並促進DNA複製初期的起始點活化反應】